|
||||||||||||||||||||||||||||
![]()
|
Nombre de masse & Numéro atomique |
|
|
|
|
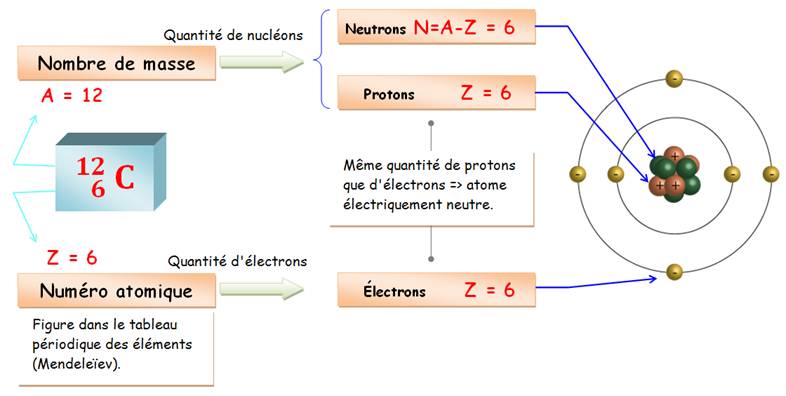
Exemple
avec le carbone-12
Anion: du grec ana-, en haut et iôn, qui va. Atome avec
électrons en surnuméraire, donc chargé négativement. Il est attiré par une
électrode positive (anode). Cation: du grec cata-, en bas et iôn, qui va. Atome avec
électrons en déficit, donc chargé positivement. Il est attiré par une
électrode négative (cathode). Mnémotechnique: Anion = négatif, on
peut retenir: Ah, non! c'est négatif; Cation =
positif, on peut retenir: pause caca. Voir Anode
et cathode Sel
de cuisine NaCl: Na+ est le cation et Cl-
est l'anion. Voir DicoMot / Liaison ionique |
|
Voir Tableau périodique donnant le numéro
atomique / Carbone / Plomb
|
|
|
|
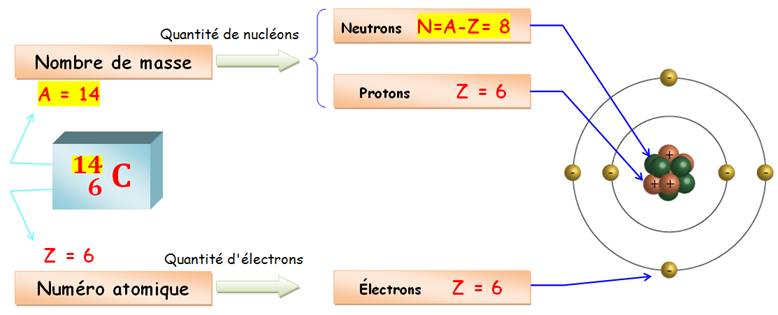
Exemple
avec le carbone-14
isotope du carbone
|
|
Voir Le cinquième cavalier -
Isotope
|
|
||||||
|
|
|
Nb de masse Nucléons |
Neutrons |
Protons |
N° atomique Électrons |
|
|
NATURELS |
|
A |
N |
Z |
Z |
|
|
Carbone |
12 6 C |
12 |
6 |
6 |
6 |
|
|
Oxygène |
16 8 O |
16 |
8 |
8 |
8 |
|
|
Cuivre |
63 34 Cu |
63 |
29 |
34 |
34 |
|
|
Or |
197 79 Au |
197 |
118 |
79 |
79 |
|
|
ISOTOPES |
|
A et N différents |
Z identiques |
|||
|
Hydrogène |
1 1 H |
1 |
0 |
1 |
1 |
|
|
Deutérium |
2 1 H |
2 |
1 |
1 |
1 |
|
|
Tritium |
3 1 H |
3 |
2 |
1 |
1 |
|
Voir Isotopes
/ Diverses sortes d'eaux
|
|
||
|
Nombre de masse |
|
|
|
Masse atomique |
|
|
|
Poids atomique |
|
|
|
|
||
|
Première fission 1932 George
Gamow (1904-1968) John Cockroft Ernest
Walton |
|
|
Source: Il était sept fois la révolution –
Étienne Klein – Flammarion – page 35
![]()
|
Retour |
|
|
Voir |
|
|
Aussi |
|
|
Source |
|
|
Cette page |
http://villemin.gerard.free.fr/aScience/PhyNucle/NbMasse.htm |